丂俋亅俇丗媡揮幨傪夘偟偨僼傽乕僕tail fiber偺曄堎
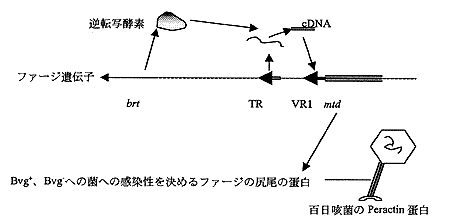
丂Bordetena pertussis偼昐擔奝偺婲場嬠偱偁傞丅婥摴偵姶愼偟偦偙偱憹怋偟側偗傟偽側傜側偄丅偟偐偟丄偦偺堊偵偼丄嬠偼婥摴擲枌偵偟偭偐傝傊偽傝晅偔昁梫偑偁傞丅偮傑傝惗懱撪偱憹怋偡傞偵偼丄嵶嬠偺愙拝場巕偑廳梫側栶妱傪壥偨偡丅堦曽丄娐嫬拞偱偺憹怋偵偼偦偺傛偆側場巕偼晄梫偱偁傞丅偦偙偱丄昐擔奝嬠偼pertactin偲塢偆愙拝場巕傪敪尰偟偰偄傞Bvg+偲塢偆憡偲丄偙傟傪敪尰偟側偄Bvg-偲塢偆憡偺娫傪峴偒棃偟偰偄傞丅張偱丄pertactin偼BPP-1偲塢偆僶僋僥儕僆僼傽乕僕偺儗僙僾僞乕偱傕偁傞丅偮傑傝丄BPP-1僼傽乕僕偼昦尨惈偺偁傞Bvg+憡偺嬠偵偼姶愼偡傞偑丄昦尨惈偺側偄Bvg-偵偼姶愼偟側偄丅
丂BBP-1僼傽乕僕傪Bvg-偺嬠偵姶愼偝偣傞偲丄彮悢側偑傜丄姶愼偑惉棫偡傞曄堎僼傽乕僕偑弌偰棃傞丅偙偺傛偆側曄堎僼傽乕僕偵偼Bvg-偺嬠偵偟偐姶愼偟側偄傕偺偲Bvg-丄Bvg+椉曽偺嬠偵姶愼偡傞傕偺偲偑偁傞丅僱僘儈僠僼僗嬠偺憡曄堎偺傛偆側f1ip-flop偱偼側偄丅
丂偙偺傛偆側僼傽乕僕偱偼壗張偵曄堎偑婲偙偭偰偄傞偺偱偁傠偆偐丅挷傋傞偲嬠傊偺媧拝偵巊傢傟傞怟旜偺抈敀Mtd偵傾儈僲巁曄堎偑婲偙偭偰偄傞丅偟偐傕丄曄堎偺応強偼怟旜抈敀Mtd抈敀偺C枛44傾儈僲巁攝楍晹暘(堚揱巕忋偱偼134bp偺VR1椞堟)偵尷掕偝傟丄曄堎偡傞傾儈僲巁傕22偺摿掕側晹埵偵尷傜傟偰偄傞丅旕忢偵晄巚媍側曄堎偺婲偙傝曽偱偁傞丅
丂偙偺曄堎偵偼2偮偺堚揱巕椞堟偑娭梌偟偰偄傞偙偲偑暘偐偭偨丅堦偮偼丄Mtd抈敀傪僐乕僪偡傞堚揱巕(mtd)偺壓棳偵偁傞TR(temp1ate
repeat)偲屇偽傟傞椞堟偱丄忋婰134bp偺VR1椞堟偲杦偳摨偠墫婎攝楍傪偟偰偄傞丅傕偆堦偮偼brt偲塢偆椞堟偱丄尨妀嵶朎偺媡揮幨峺慺偱儗僩儘僂僀儖僗偺媡揮幨峺慺偲憡摨側堚揱巕偱偁傞丅brt傪晄妶壔偡傞偲僼傽乕僕偺曄堎偑婲偙傜側偔側傞丅嫲傜偔brt堚揱巕嶻暔偑TR偺揮幨嶻暔傪媡揮幨偟丄偙偺cDNA偑壗傜偐偺偐偨偪偱VR1椞堟偵庢傝崬傑傟曄堎傪婲偙偡偺偱偁傠偆丅
丂偦傟偱偼丄怓乆側曄堎偼偳偆偟偰婲偙傞偺偱偁傠偆偐?
曄堎偺婲偙傞22偺応強偼TR偱偼慡偰傾僨僯儞巆婎偲側偭偰偄傞丅偙傟傜傾僨僯儞偺晹埵偱丄媡揮幨偺嵺偵丄岆偭偨墫婎傪堎忢偵庢傝崬傒堈偄偐丏埥偄偼丄墫婎偺廋忺偑婲偙傞寢壥偱偼側偄偐偲巚傢傟傞
(Science 295 2031-2032.2002)
丂
9-7:惗暔奅偵墬偗傞摦偒夞傞堚揱巕
丂愭偵丄IS丄Tn偺傛偆側嵶嬠偺愼怓懱傗僾儔僗儈僪忋傪摦偒夞傞堚揱巕偵偮偄偰弎傋偨丅嵶嬠丄怉暔丄僸僩傪娷傓怓乆側摦暔偺僎僲儉夝愅偑恑傓偵偮傟丄偙偺傛偆側摦偒夞傞堚揱巕偼惗暔偺堚揱巕偺拞偵斆棓偟偰偄傞偙偲偑暘偐偭偰偒偨丅偙傟偼丄C-value
paradox偲塢偆傕偺偲娭學偑偁傞丅
丂C-value
paradox偲偼乽惗暔偺帩偮DNA偺戝偒偝偑恑壔搙偲堦抳偟側偄乿偲塢偆尰徾偱偁傞丅椺偊偽丄Amoeba proteus偲塢偆尨拵偺DNA偼29亊1010墫婎懳傕偁傞偺偵丄僸僩偼34亊108偱偁傝丄拵偺100暘偺侾偺戝偒偝偟偐側偄丅僸僩偺堚揱忣曬偑尨拵偺100暘偺侾偱偁傞偲偼峫偊偵偔偄丅嫲傜偔偼丄尨拵偺DNA偺戝晹暘偼桳梡側堚揱忣曬傪帩偨側偄僑儈乮junk乯偱偼側偄偐偲塢傢傟偰偒偨丅
丂僎僲儉夝愅偵傛傝丄偙偺傛偆側悇掕偑惓偟偐偭偨偙偲偑師戞偵柧傜偐偵偝傟偮偮偁傞丅椺偊偽丄僸僩偺
DNA偺拞偱抈敀傪僐乕僪偟偰偄傞偺偼慡懱偺1.5%埵偱丄堚揱巕偺悢偵偟偰40,000埵丄彮側偔偲傕慡懱偺45%偼抈敀傪僐乕僪偟側偄摦偔堚揱巕偵桼棃偡傞DNA偱偁傞丅怉暔偺Arabidopsis
thaliana偵側傞偲丄柍懯側晹暘偑彮側偔側傝丄DNA偺39%偑抈敀傪僐乕僪偟丄堚揱巕悢偼25,498偲偝傟偰偄傞丅懠曽丄峺曣偱偼70%偺DNA偑抈敀傪僐乕僪偟乮堚揱巕悢6340乯丄junk晹暘偑彮側偔丄柍懯偺側偄峔憿偵側偭偰偄傞丅尨妀嵶朎偵側傞偲峏偵柍懯偑柍偔側傝85-95%偑僐乕僪椞堟偲側傞丅懡偔偺恀妀嵶朎惗暔偼壗屘偙偺傛偆偵柍懯側DNA傪攚晧偄崬傫偱偄傞偺偩傠偆偐丅
9-7-1:恀妀嵶朎偺摦偔堚揱巕
丂摦偔堚揱巕偵偼丄RNA傊偺揮幨偲偦傟偐傜偺DNA傊偺媡揮幨傪夘偡傞傕偺偲丄嵶嬠偺IS傗Tn偺傛偆偵DNA暘巕偲偟偰摦偒夞傞堚揱巕偑偁傞丅慜幰傪儗僩儘僩儔儞僗億僜儞乮retrotransposon乯丄屻幰傪DNA僩儔儞僗億僜儞偲塢偆丅
乮侾乯儗僩儘僩儔儞僗億僜儞
丂儗僩儘僩儔儞僗億僜儞偵偼丄儗僩儘僂僀儖僗摨條LTR傪僎僲儉椉抂偵帩偮傕偺偲LTR傪帩偨側偄傕偺偑偁傞丅慜幰傪LTR transposon丄屻幰傪non-LTR
transposon偲塢偆丅
丂LTR僩儔儞僗億僜儞偼丄Ty1-copia偲Ty3-gypsy偺俀孮偵暘偗傜傟傞丅Ty1偲Ty3偼峺曣丄copia偲gypsy偼僔儑僂僕儑僂僶僄乮Drosophila
melanogaster乯偱敪尒偝傟偨傕偺偱偁傞丅恾9-7-(1)偵柾幃恾傪帵偡丅Env堚揱巕偼丄Ty1-copia偵偼柍偄丅Ty3-gypsy偵偺傒懚嵼偡傞丅

恾9-7-(1)
Ty3-gypsy偼Env傪帩偮偺偱丄儗僩儘僂僀儖僗摨條偺揱斃宍幃傪庢傞偲巚傢傟傞偑丄Ty1-copia偵傕悈暯揱払偺偁傞偙偲偑徹柧偝傟偰偄傞丅嫲傜偔丄Ty3-gypsy偺Env偵傛傝曪傒崬傑傟僂僀儖僗棻巕偲偟偰暿偺庬偵姶愼偡傞偲巚傢傟傞丅Ty1-copia僞僀僾偼Env柍偟偵堦偮偺嵶朎偺拞偱愼怓懱忋傪摦偒夞傞帠偑弌棃傞丅偟偐偟丄Gag抈敀偼帩偭偰偄傞丅偙偺帠偼Gag抈敀偼摦偒夞傞堊偵昁恵偱偁傞偙偲傪帵偟偰偄傞偺偐傕抦傟側偄丅儗僩儘僂僀儖僗偺僾儘僂僀儖僗慻傒崬傒暋崌懱偑Gag抈敀傪娷傫偱偄傞帠傪峫偊傞偲丄偦偺壜擻惈偼崅偄丅
丂LTR儗僩儘僩儔儞僗億僜儞偺摿挜偼慻傒崬傒晹埵偵摿堎惈偺偁傞揰偱偁傞丅峺曣偺Ty1偼丄Pol
III偱揮幨偝傟傞堚揱巕乮tRNA偲堦晹rRNA乯偺忋棳悢昐墫婎偺張偵屌傑偭偰慻傒崬傑傟偰偄傞丅偙傟偼丄峺曣DNA偺俈妱偑僐乕僪椞堟偱偁傝丄偱偨傜傔偵慻傒崬傑傟傞偲峺曣偵偲偭偰抳巰揑偵側傝偊傞帠
偲娭學偑偁傞偐傕抦傟側偄丅幚嵺Ty1偺慻傒崬傒晹埵傪挷傋偰傒傞偲抈敀傪僐乕僪偡傞堚揱巕偺拞偵懚嵼偡傞傕偺偼侾偮傕側偄丅
恾9-7-(2)丗Non-LTR儗僩儘億僜儞
丂Non-LTR僩儔儞僗億僜儞偵偼LINE (long interspersed nuclear
elements)偲SINE (short interspersed nuclear elements)偲偑偁傞丅SINE偵偼僸僩偺Alu攝楍偑偁傝丄僸僩僎僲儉偺10.6%傪愯傔傞乮恾9-7-(2)乯丅
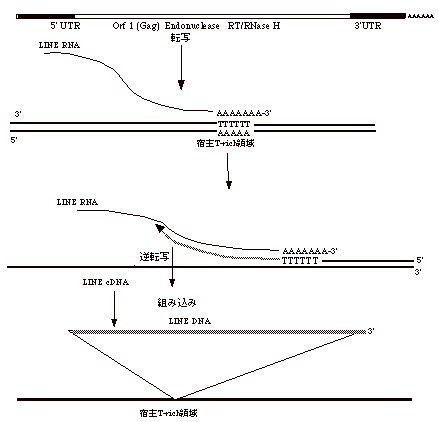
丂LINE 偼丄RNA偵揮幨偝傟傞偲慻傒崬傒暋崌懱偲側傝丄偦偺Endonuclease偑愼怓懱DNA偺T-rich側晹暘傪愗抐偟丄3乫
偺poly-A攝楍丄(A)5-11丄偵傛傝T-rich側攝楍偲hybridize偡傞丅愗抐偝傟偨愼怓懱DNA偺T-rich攝楍傪primer偵偟偰偦偙偐傜LINE僎僲儉傪媡揮幨偟cDNA傪崌惉偡傞丅偙偺摿挜偼丄RNA偐傜DNA傊偺媡揮幨偑僩儔儞僗億僜儞偺慻傒崬傒偲僇僢僾儖偟偰偄傞揰偱偁傞丅3乫懁偐傜媡揮幨偑婲偙傞偨傔丄搑拞偱揮幨偑巭傑傝丄慻傒崬傑傟偨LINE僎僲儉偼丄5乫抂傪寚懝偡傞応崌偑懡偄丅
丂 HTLV-1偺慻傒崬傒晹埵傪挷傋傞偲敿悢嬤偔偑5乫抂傪寚偔僾儘僂僀儖僗偱偁傞乮Hiramatsu &
Yoshikura, J. Virol. 58, 508-512乯丅HTLV-1偼揟宆揑側LTR傪帩偮儗僩儘僂僀儖僗偱偁傞偑丄Non-LTR儗僩儘億僜儞偲嫟捠偟偨慻傒崬傒宱楬傪帩偮偺偐傕抦傟側偄丅
乮俀乯DNA僩儔儞僗億僜儞
丂 愼怓懱 DNA忋偵懚嵼偡傞僩儔儞僗億僜儞堚揱巕偑丄RNA傊偺揮幨傪夘偝偢偵丄摦偒夞傞揰偱丄嵶嬠偺IS傗Tn偵帡偰偄傞丅僩儔儞僗億僕僔儑儞偼丄嵶嬠偺class
I僩儔儞僗億僜儞偲摨偠偔愗傝弌偝傟丄捈愙丄廻庡DNA偵慻傒崬傑傟傞non-replicative type
偺傕偺偱偁傞丅廬偭偰丄僩儔儞僗億僜儞DNA偑愗傝弌偝傟偨屻偺DNA偺廋暅偑昁梫偵側傝丄偙傟偑柍偄偲偦偙偵擇廳嵔愗抐傪巆偟丄廻庡偵偲偭偰抳柦揑偵側傝摼傞丅
丂Tc1/mariner僩儔儞僗億僜儞
丂Tc1偼C. elegans偱丄mariner偼Drosophila偱尒偮偐偭偨僩儔儞僗億僜儞偱偁傞丅DNA僩儔儞僗億僜儞偺拞偱嵟傕扨弮側峔憿傪偟偰偍傝丄僒僀僘傕1.6-2.3kb偲斾妑揑彫偝偄丅僎僲儉偺椉抂偵媡岦偒孞傝曉偟攝楍乮IR乯偑偁傝丄IR偵嫴傑傟偰僩儔僗億僛乕僗堚揱巕偑偁傞丅廬偭偰丄嵶嬠偺IS偵傛偔帡偰偄傞丅Transposition偼僩儔儞僗億僜儞偑愼怓懱偐傜愗傝弌偝傟丄怴偟偄応強偵慻傒崬傑傟傞偙偲偵傛傝婲偙傞丅慻傒崬傑傟傞晹埵偺墫婎攝楍偼5乫-TA-3乫偱丄儗僩儘僂僀儖僗偺慻傒崬傒偺応崌偲摨條抜堘偄愗抐乮staggered
cut乯偑擖傞堊丄慻傒崬傑傟偨僩儔儞僗億僜儞偺椉抂偵廻庡愼怓懱桼棃偺AT攝楍偑尒傜傟傞丅堦曽丄僩儔儞僗億僜儞偑愗傝弌偝傟偨屻偺愼怓懱晹埵偼丄blunt
end ligation乮抐抂寢崌乯傗憡摨慻傒懼偊側偳偵傛傝廋暅偝傟傞丅
丂俹場巕乮P-element乯偼Tc1/mariner偺拠娫偱偁傞丅偙偺場巕偼hybrid
dysgenesis偲塢偆尰徾傪夘偟偰敪尒偝傟偨丅懄偪丄俹場巕傪帩偮梇偺僔儑僂僕儑僂僶僄偲俹場巕傪帩偨側偄帗傪妡偗崌傢偣傞偲巕懛偑弌棃側偄丅偟偐偟丄俹場巕傪帩偮梇傪俹場巕傪帩偮帗偵妡偗崌傢偣傞偲巕懛偑弌棃傞丄偲塢偆尰徾偱偁傞丅
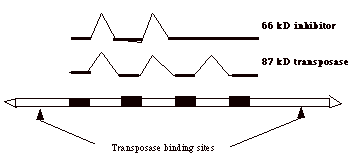
恾9-7-(3)丗俹場巕偲偦偺揮幨嶻暔
丂俹場巕偺堚揱巕偺椉抂偵偼31墫婎懳媡岦偒孞傝曉偟峔憿偑偁傝丄IRBP偲塢偆廻庡桼棃偺僩儔儞僗億僕僔儑儞偵娭梌偡傞抈敀偑寢崌偡傞丅偙偺抈敀偼俀廳嵔DNA愗抐偺廋暅偵娭梌偡傞峺慺偱偁傞丅偦偺撪懁偵偦傟偧傟transposase偺寢崌晹埵偑偁傞丅
丂P場巕偺Transposase偺堚揱巕偼丄僩儔儞僗億僜儞偺恀傫拞偵偁傝丄俁偮偺intron丄懄偪係偮偺exon偐傜側傞丅
丂Transposase偺mRNA偺姰慡側僗僾儔僀僔儞僌偼惗怋嵶朎偱偺傒婲偙傝丄懱嵶朎偱偼晄姰慡偱偁傞丅懄偪丄俁斣栚偺intron偺splice
out偑婲偙傜側偄丅偙傟偼丄懱嵶朎偱偼偙偺僗僾儔僀僔儞僌傪墴偝偊傞場巕PSI偑敪尰偟偰偄傞堊偱偁傞丅偙偺堊丄惗怋嵶朎偩偗偱妶惈偺偁傞87kD偺transposase傪僐乕僪偡傞mRNA偑揮幨偝傟丄惗怋嵶朎偩偗偱俹場巕堚揱巕偑旘傃夞傟傞丅
丂堦曽丄俁斣栚偺intron偑splice out偝傟側偄mRNA偼66kD偺抈敀傪僐乕僪偟丄嫲傜偔transposase偑寢崌偡傞晹埵乮椉抂IR偺捈偖撪懁偵偁傞乯偵嫞崌揑偵寢崌偡傞偨傔丄transposase傪梷惂偡傞丅俹場巕傪帩偮帗偺嵶朎偱偼偙偺66kD抈敀偑懡検偵拁愊偝傟偰偄傞丅偦偙偱丄P場巕傪帩偮帗偺棏偵梇偺DNA偑摫擖偝傟傞偲丄66kD抈敀偑梇偺俹場巕偑敪尰偡傞transposase傪梷惂偡傞丅堦曽丄俹場巕傪帩偨側偄帗偲偺妡偗崌傢偣偱偼丄棏偵偼66kD抈敀偼拁愊偝傟偰偄側偄偺偱丄俹場巕偺transposase偑偦偺傑傑妶惈壔偟惙傫偵transposition偑婲偙傞丅寢壥丄屻偺慻傒崌傢偣偱偺傒transposition偵傛傞愼怓懱DNA偺彎奞偑婲偙傝丄巕懛偑弌棃側偄偙偲偵側傞丅
丂hAT僼傽儈儕乕
丂McClintock偑敪尒偟偨Ac transposon偑偙偺拠娫偵擖傞丅11墫婎懳偺媡岦偒孞傝曉偟攝楍偑偁傝丄偦偺撪懁偵係偮偺intron傪帩偮transposase堚揱巕偑偁傞丅堚揱巕偺戝偒偝偼4.6kb偱偁傞丅
Ac偺懠偵丄幦柾條偺僉儞僊儑僜僂偺壴偺尨場偱偁傞Tam丄俹場巕摨條hybrid dysgenesis傪婲偙偡hobo偑偁傞丅愗傝弌偝傟偨屻偺愼怓懱DNA偑hairpin傪嶌傞摿挜偑偁傞丅柶塽宯偺嵶朎偱DNA嵞攝楍偺嵺偺RAG1丄RAG2偵傛傞VDJ慻傒懼偊偱hairpin峔憿偑弌棃傞揰傛偔帡偰偄傞丅偙偺堊丄妉摼柶塽偵墬偗傞DNA慻傒懼偊偺婲尮偼悈暯揱払偵傛傝妉摼偝傟偨transposon偵偁傞偺偱偼側偄偐偲塢傢傟偰偄傞丅
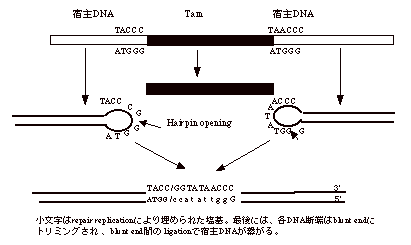
恾9-7-(4)丗hTA僼傽儈儕乕
丂
乮俁乯僩儔儞僗億僜儞偺摑崌揑側峫偊曽
丂忋偵弎傋偨傛偆偵庬乆偺僩儔儞僗億僕僔儑儞偑偁傞丅transposon偺暋惢偲慻傒崬傒偑嫟栶偟偰偄傞replicative側傕偺乮Tn3偺傛偆側class
II transposon乯丄偨偩愗傝弌偝傟愼怓懱偺暿偺晹埵偵憓擖偝傟傞non-replicative側傕偺乮P element丄Ac
transposon摍乯偑偁傞丅枖丄儗僩儘僂僀儖僗偺姶愼偱偼慻傒崬傒偺慜嬱懱偵偼側傝摼側偄偲巚傢傟傞娐忬僾儘僂僀儖僗偑弌棃傞丅偦傟偧傟僶儔僶儔偱壗偺嫟捠惈傕柍偄傛偆偵尒偊傞丅
丂偙偙偱拲堄偟偨偄偺偼丄DNA偑愼怓懱 DNA偵慻傒崬傑傟傞帪丄DNA transposon偺応崌偵偼transposase丄LTR儗僩儘億僜儞偺応崌integrase丄non-LTR儗僩儘億僜儞偺応崌endonuclease摍僩儔儞僗億僜儞DNA偲僩儔儞僗億僜儞偑僐乕僪偡傞抈敀丄廻庡抈敀偑暋崌懱偲側偭偨傕偺偑昗揑廻庡DNA偲憡屳嶌梡傪偡傞偲塢偆偙偲偱偁傞乮恾9-7-(5)乯丅
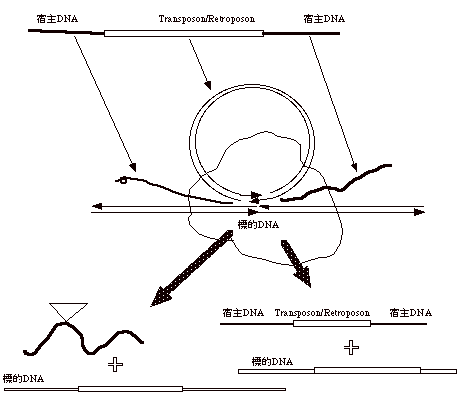
丂懄偪丄婎杮揑偵偼transposon
complex偲塢偆傋偒暋崌懱傪夘偟丄庬乆側慻傒懼偊嶻暔偑弌棃偰偄傞丅偙偺條側暋崌懱偺摿挜偼丄慻傒姺偊偵娭梌偡傞DNA摨巑偺嫬奅晹暘丄偮傑傝偍屳偄偵慻傒姺偊崌偆DNA晹暘偑丄暋崌懱偺拞偱嬤愙偟偨忬懺偵側傞帠偱偁傞丅慻傒姺偊嶻暔偺偐偨偪偼丄偳偺DNA嵔偺抐抂偲丄偳偺DNA嵔偺抐抂偑楢寢偝傟傞偐偱寛傑傞丅偦偺慻傒崌傢偣傪寛傔傞偺偑transposase埥偄偼integrase偱偁傞丅廬偭偰丄婎杮揑側儊僇僯僘儉偼庬乆偺僩儔儞僗億僜儞娫偱嫟捠偟偰偄傞偲傕塢偊傞丅丂
(4)
摦偒夞傞Intron
splicing偵偼丄恀妀嵶朎偺mRNA偺 splicing乮戞俇復嶲徠乯埲奜偵丄尨妀嵶朎傗儈僩僐儞僪儕傾偱尒傜傟傞Group I丄Group
II偺splicing偑偁傞丅慜幰丄懃偪丄恀妀嵶朎偺mRNA偺splicing偼妀撪偱RNA偲抈敀偺暋崌懱spliceosome偵傛傝峴傢傟in
vivo偱偺傒娤嶡偝傟傞偑丄Group I splicing乮僥僩儔僸儊僫偺rRNA偱尒傜傟傞乯埥偄偼Group II
splicing乮僥僩儔僸儊僫偺儈僩僐儞僪儕傾mRNA偱尒傜傟傞乯偼in
vivo偱偁傞帠傪昁偢偟傕昁梫偲偣偢丄帋尡娗撪偱RNA帺恎偺峺慺妶惈乮Rybozyme妶惈乯偵傛傝婲偙傞丅
嵟嬤丄偙偺Group I埥偄偼Group II偺intron偺拞偵僩儔儞僗億僜儞偺條偵摦偒夞傞intron偺偁傞帠偑暘偐偭偰偒偨丅偙偺傛偆側intron偵偼僐乕僪椞堟乮open
reading frame, ORF乯偑偁傞丅ORF偼丄昗揑DNA偵愗傝崬傒傪擖傟傞endonuclease丄intron
RNA偐傜DNA傪媡揮幨偡傞reverse transcriptase丄RNA慜嬱懱偐傜摿掕偺intron晹暘傪愗傝弌偡峺慺maturase丄偺堚揱巕偑偁傞丅
椺偊偽丄峺曣偵偼冎亄偲冎—偺擇庬椶偺姅偑偁傝丄慜幰偵偼group I intron偑偁傞偑屻幰偵偼側偄丅岎攝偡傞偲巕懛(haploid偱偁傞偙偲偵拲堄)偼昁偢冎亄偲側傞丅懃偪丄岎攝偵傛傝冎—姅偵group
I intron偑堏偭偨偲峫偊傜傟傞丅張偑丄冎亄嵆偼冎—偺曄堎偵傛傝丄岎攝偱冎亄偲冎—偺巕懛偑摨悢弌棃傞傛偆側曄堎姅偑尒偮偐偭偨丅挷傋偰傒傞偲丄曄堎偑冎—偺懁偵偁傞応崌偺曄堎晹埵偼intron偑憓擖偝傟傞晹埵偺朤偱偁傝丄曄堎偑冎亄偺懁偵偁傞応崌偵偼曄堎偼intron撪偺僐乕僪椞堟乮ORF乯偵偁偭偨丅偙偺ORF偼intron偑憓擖偝傟傞昗揑DNA偵俀墫婎偺抜堘偄愗傝崬傒乮staggered
cut乯傪擖傟傞endonuclease傪僐乕僪偟偰偄偨丅嫲傜偔丄intron
RNA傪拻宆偲偟偰DNA偑崌惉偝傟丄俀偮偺愗抐晹埵偺娫偵擖傝崬傓偺偱偁傠偆丅憓擖晹埵偼堦掕側偺偱偙傟傪intron homing偲塢偆丅
Group II intron偼intron偵摿堎惈偺偁傞媡揮幨峺慺傪僐乕僪偟偰偄偰丄non-LTR
僩儔儞僗億僜儞偲摨條側婡峔乮6-7-1(1)嶲徠乯偱慻傒崬傑傟傞偲峫偊傜傟偰偄傞丅抈敀嶻暔傪娷傓儕儃妀巁抈敀偲婎幙偲側傞DNA傪帋尡娗撪偱斀墳偝偣傞偲丄Group
II intron偺婎幙DNA傊偺憓擖偑婲偙傞丅